Доброе время суток, уважаемые десятиклассники!
Мы начинаем знакомиться с новой группой органических соединений - углеводами.
Углеводы... А это те самые сладости, которые вы так любите, (фрукты, торты, конфеты, варенье, шоколад и т.д., особенно много углеводов содержит виноград). Углеводы жизненно важные вещества, которые необходимы каждому организму. Эти вещества расходуются, и человек должен постоянно пополнять их запасы. Понятно, что вещества, входящие в состав тканей организма, не похожие на те, которые он употребляет в пищу. Организм человека перерабатывает пищевые продукты и в процессе своей жизнедеятельности постоянно расходует энергию, которая, как мы знаем, выделяется при окислении в тканях организма, углеводы входят в состав нуклеиновых кислот, осуществляющих биосинтез белка и передачу наследственных признаков.
Животные и человек не синтезируют углеводы. В зеленых растениях при участии хлорофилла и солнечного света осуществляется ряд процессов преобразования поглощенной из воздуха углекислого газа и впитанной из почвы воды. Конечным продуктом этих процесса – фотосинтеза, является сложная молекула углевода.
Углеводы – важный источник энергии для организма, участвуют в обмене веществ. Основными источниками углеводов являются растительные продукты.
Углеводы... А это те самые сладости, которые вы так любите, (фрукты, торты, конфеты, варенье, шоколад и т.д., особенно много углеводов содержит виноград). Углеводы жизненно важные вещества, которые необходимы каждому организму. Эти вещества расходуются, и человек должен постоянно пополнять их запасы. Понятно, что вещества, входящие в состав тканей организма, не похожие на те, которые он употребляет в пищу. Организм человека перерабатывает пищевые продукты и в процессе своей жизнедеятельности постоянно расходует энергию, которая, как мы знаем, выделяется при окислении в тканях организма, углеводы входят в состав нуклеиновых кислот, осуществляющих биосинтез белка и передачу наследственных признаков.
Животные и человек не синтезируют углеводы. В зеленых растениях при участии хлорофилла и солнечного света осуществляется ряд процессов преобразования поглощенной из воздуха углекислого газа и впитанной из почвы воды. Конечным продуктом этих процесса – фотосинтеза, является сложная молекула углевода.
Углеводы – важный источник энергии для организма, участвуют в обмене веществ. Основными источниками углеводов являются растительные продукты.
Физиологи установили, что при физической нагрузке, которая в 10 раз превышает привычную, человек, соблюдающий жировую диету, лишается сил уже через полчаса. А вот углеводная диета позволяет выдержать такую же нагрузку в течение четырех часов. Оказывается, получение организмом энергии из жиров – процесс длительный. Это объясняется малой реакционной способностью жиров, особенно их углеводородных цепей. Углеводы же, хотя и дают меньше энергии, чем жиры, однако выделяют ее намного быстрее. Поэтому, если предстоит основательная нагрузка, предпочтительнее подкрепиться сладким, а не жирным.
Классификация углеводов.
Углеводы – обширный класс природных соединений.Обратимся к схеме 1. “Классификация углеводов”. В зависимости от числа остатков моносахаридов в молекуле делятся на моносахариды, дисахариды и полисахариды.
Моносахариды (простые углеводы) – углеводы, которые не гидролизуются. В зависимости от числа атомов углерода подразделяются на триозы, тетрозы, пентозы, гексозы. Для человека наиболее важны глюкоза, фруктоза, галактоза, рибоза, дезоксирибоза.
Дисахариды – углеводы, которые гидролизуются с образованием двух молекул моносахаридов. Наиболее важны для человека сахароза, мальтоза и лактоза.
Полисахариды – высокомолекулярные соединения – углеводы, которые гидролизуются с образованием множества молекул моносахаридов. Они делятся на перевариваемые и неперевариваемые в желудочно-кишечном тракте. К перевариваемым относят крахмал и гликоген, из вторых для человека важны клетчатка, гемицеллюлоза и пектиновые вещества.
Углеводы часто называют сахаристыми веществами или сахарами. Они могут быть безвкусными, сладкими и горькими. Если сладость раствора сахарозы принимать за 100 %, то сладость фруктозы – 173 %, глюкозы – 81 %, мальтозы и галактозы – 32 %, лактозы – 16 %.
Качественный состав углеводов.
Углеводы – органические соединения, состоящие из углерода, водорода и кислорода, причем водород и кислород входят в соотношении (2 : 1) как в воде, отсюда и название.
На основе этой аналогии русский химик К. Шмидт в 1844 г. предложил термин углевода (углерод и вода), а общая формула углеводов Сn(Н2О)m
Итак, важнейшим представителем моносахаридов является глюкоза. При изучении, каких некоторых тем мы встречались с вами с этим веществом в курсе химии и биологии: химия – альдегиды, спирты; биология – фотосинтез, строение клетки.
Получение глюкозы.
1. Реакция фотосинтеза.6СО2 + 6H2O –> С6Н12 О6 + 6О2 +Q
2. Реакция полимеризации.
3. Гидролиз крахмала.
(С6Н10О5)n + nH2O –> nС6Н12О6
Физические свойства:
Строение молекулы глюкозы. Изомерия.
Вывод: таким образом, глюкоза – альдегидоспирт, точнее – многоатомный альдегидоспирт.Установлено, что в растворе глюкозы находится не только её альдегидная форма; но и молекулы циклического строения.
Установлено, что у третьего атома углерода группа – ОН расположена иначе, чем у других атомов углерода распространённое строение глюкозы выглядит так:
Превращение молекулы линейного строения в молекулу циклического строения объяснимо, если вспомнить что атомы углерода могут вращаться вокруг сигма -связей. Альдегидная группа может приблизиться к гидроксильной группе 5-го атома углерода, поскольку атом кислорода карбонильной группы несёт на себе частичный – заряд, а атом водород гидроксильной группы – частично + заряд.
Осуществляется своеобразный химический процесс: происходит разрыв -связи карбонильной труппы, к атому кислорода присоединяется атом водорода, а атом кислорода гидроксильной группы с атомом углерода замыкают цепь. Циклические формы находятся в равновесии, превращаясь альфа и бетту форму. Таким образом, в водном растворе глюкозы находятся три изомерные формы. Молекула кристаллической глюкозы альфа -форма, при растворении в воде – открытая форма, а затем снова циклическая бетта-форма. Такая изомерия называется динамической (таутомерия).
Химические свойства глюкозы.
Моносахариды вступают в химические реакции, свойственные карбонильной и гидроксильной группам.
1) Реакция “серебряного зеркала”
Доказать наличие альдегидной группы в глюкозе можно с помощью аммиачного раствора оксида серебра. Эта реакция называется реакцией серебряного зеркала. Ее используют как качественную для открытия альдегидов. Альдегидная группа глюкозы окисляется до карбоксильной группы. Глюкоза превращается в глюконовую кислоту.
СН2ОН – (СНОН)4 – СОН + Ag2O = СН2ОН – (СНОН)4 – СООН + 2Ag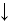
(Реакцию серебряного зеркала используют в промышленности для серебрения зеркал, изготовления колб для термосов, елочных украшений).
2) Взаимодействие глюкозы с гидроксидом меди (II)
Установлено, что у третьего атома углерода группа – ОН расположена иначе, чем у других атомов углерода распространённое строение глюкозы выглядит так:
Превращение молекулы линейного строения в молекулу циклического строения объяснимо, если вспомнить что атомы углерода могут вращаться вокруг сигма -связей. Альдегидная группа может приблизиться к гидроксильной группе 5-го атома углерода, поскольку атом кислорода карбонильной группы несёт на себе частичный – заряд, а атом водород гидроксильной группы – частично + заряд.
Осуществляется своеобразный химический процесс: происходит разрыв -связи карбонильной труппы, к атому кислорода присоединяется атом водорода, а атом кислорода гидроксильной группы с атомом углерода замыкают цепь. Циклические формы находятся в равновесии, превращаясь альфа и бетту форму. Таким образом, в водном растворе глюкозы находятся три изомерные формы. Молекула кристаллической глюкозы альфа -форма, при растворении в воде – открытая форма, а затем снова циклическая бетта-форма. Такая изомерия называется динамической (таутомерия).
Химические свойства глюкозы.
Моносахариды вступают в химические реакции, свойственные карбонильной и гидроксильной группам.
1) Реакция “серебряного зеркала”
Доказать наличие альдегидной группы в глюкозе можно с помощью аммиачного раствора оксида серебра. Эта реакция называется реакцией серебряного зеркала. Ее используют как качественную для открытия альдегидов. Альдегидная группа глюкозы окисляется до карбоксильной группы. Глюкоза превращается в глюконовую кислоту.
СН2ОН – (СНОН)4 – СОН + Ag2O = СН2ОН – (СНОН)4 – СООН + 2Ag
(Реакцию серебряного зеркала используют в промышленности для серебрения зеркал, изготовления колб для термосов, елочных украшений).
2) Взаимодействие глюкозы с гидроксидом меди (II)
3) Гидрирование глюкозы
Альдегидная группа может быть восстановлена в гидроксильную группу действием водорода в присутствии катализатора.
4) Специфические свойства.Большое значение имеют процессы брожения глюкозы, происходящие под действием органических катализаторов-ферментов (они вырабатываются микроорганизмами).
а) спиртовое брожение (под действием дрожжей)
С6Н12О6= 2С2Н5 ОН + 2СО2
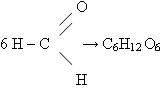
в) маслянокислое брожение
Применение глюкозы.
Глюкоза находит применение в различных отраслях промышленности:- в пищевой промышленности, как заменитель сахарозы;
- в кондитерской промышленности при изготовлении мягких конфет, десертных сортов шоколада, тортов и различных диетических изделий;
- в хлебопечении глюкоза улучшает условия брожения, придает пористость и хороший вкус изделиям, замедляет очерствение;
- в производстве мороженого она занижает точку замерзания, увеличивает его твердость;
- при производстве фруктовых консервов, соков, ликеров, вин, безалкогольных напитков, так как глюкоза не маскирует аромата и вкуса;
- в молочной промышленности при изготовлении молочных продуктов и продуктов детского питания рекомендуется использовать глюкозу в определенной пропорции с сахарозой для придания этим продуктам более высокой питательной ценности;
- в ветеринарии;
- в птицеводстве;
- в фармацевтической промышленности.
Кристаллическую глюкозу целесообразно использовать для питания больных, травмированных, выздоравливающих, а также людей, работающих с большими перегрузками.
Медицинскую глюкозу применяют в антибиотиках и других лекарственных препаратах, в том числе для внутривенных вливаний, и для получения витамина С. Техническая глюкоза находит применение в качестве восстановителя в кожевенном производстве, в текстильном – при производстве вискозы, в качестве питательной среды при выращивании различных видов микроорганизмов в медицинской и микробиологической промышленности.
Закрепление:
Источник: http://festival.1september.ru/articles/532403/







Комментариев нет:
Отправить комментарий